






«Известно, что тритерпеноиды обладают мультитаргетностью, то есть способны взаимодействовать с множеством мишеней в клетках организма, благодаря чему имеют широкий спектр биологической активности (противовоспалительную, иммуномодулирующую, противоязвенную, противоопухолевую и другие). Задача медицинской химии — создать химические производные таких соединений, которые будут связываться лишь с мишенями, определяющими развитие патологических состояний, не взаимодействуя при этом с белками, необходимыми для нормальной жизнедеятельности клетки. В лаборатории фармакологически активных веществ НИОХ СО РАН ведутся работы по синтезу таких производных, а мы изучаем их биологическую активность и устанавливаем механизмы их действия», — рассказывает научный сотрудник лаборатории биохимии нуклеиновых кислот ИХБФМ СО РАН кандидат биологических наук Андрей Владимирович Марков.
Полусинтетические тритерпеноиды, которые разрабатывают сибирские ученые, имеют в своей структуре определенные модификации, которые определяют их высокую биологическую активность. В предыдущих исследованиях производное под названием солоксолон метил (СМ) показало высокую эффективность на множестве моделей. Было установлено, что оно оказывает выраженное противоопухолевое действие — как на культурах клеток, так и в экспериментах на мышах, а также противовоспалительный эффект на модели пневмонии, вызванной вирусом гриппа. Соединение ингибировало проникновение вируса гриппа в клетку и блокировало развитие воспалительных изменений в тканях легких.
Ученые решили дополнительно модифицировать его, увеличив в составе молекулы количество групп, определявших высокую биоактивность солоксолон метила. В результате получился препарат триоксолон метил (ТМ). На макрофагах удалось показать, что он имеет более явные, чем у предшественника, противовоспалительные свойства. После чего исследователи решили испытать его на мышах. Для эксперимента была выбрана сложная модель, имитирующая язвенный колит и болезнь Крона у человека — воспаление кишечника (колит), вызванное декстрансульфатом натрия.
Солоксолон метил и триоксолон метил — это производные 18βН-глицирретовой кислоты, которая представляет собой полициклическое соединение, тритерпеноид, содержащийся в больших концентрациях в корне солодки. Поскольку исходного сырья в природе очень много, а выделение из него нужных компонентов достаточно просто, создание препаратов на основе природных тритерпеноидов является экономически выгодным направлением.
«Для того чтобы вызвать колит, мы вводили мышам декстрансульфат натрия с питьевой водой в течение семи дней и одновременно лечили их как солоксолон метилом, так и триоксолон метилом. Лечение продолжалось также в течение трех дней после введения веществ, вызывающих заболевание. Всё это время животных взвешивали и наблюдали за их внешним видом и двигательной активностью,— говорит научный сотрудник лаборатории биохимии нуклеиновых кислот ИХБФМ СО РАН кандидат медицинских наук Александра Васильевна Сенькова. — На десятые сутки мы выводили мышей из эксперимента и смотрели, какие процессы происходили в тканях кишечника и в организме в целом. Затем было проведено гистологическое исследование тканей кишечника, которое показало: наше соединение блокирует развитие патологических процессов, вызванных предварительно введенным препаратом».
Декстрансульфат натрия провоцирует не только воспаление слизистой оболочки кишечника, но и выраженное повреждение его эпителия, вплоть до формирования эрозий и язв. Триоксолон метил предотвратил развитие этих повреждений. «Мы видели выраженные эффекты нашего соединения, используя его в очень небольшой дозе, всего лишь пять миллиграмм на килограмм, и при этом не фиксировали выраженного токсического воздействия на органы и ткани, а также на организм животного в целом», — говорит Александра Сенькова.
В третьем блоке работы ученые установили возможный механизм противовоспалительного действия триоксолон метила. С помощью биоинформатических подходов они определили потенциальные мастер-регуляторы, способные контролировать развитие колита. Затем, используя молекулярное моделирование, попытались понять, способен ли триоксолон метил напрямую взаимодействовать с этими белками. В результате был выявлен ряд мишеней тритерпеноида, блокирование которых может предотвратить или остановить развитие заболевания. В том числе белки Akt и STAT3, являющиеся известными мишенями для противораковой терапии.
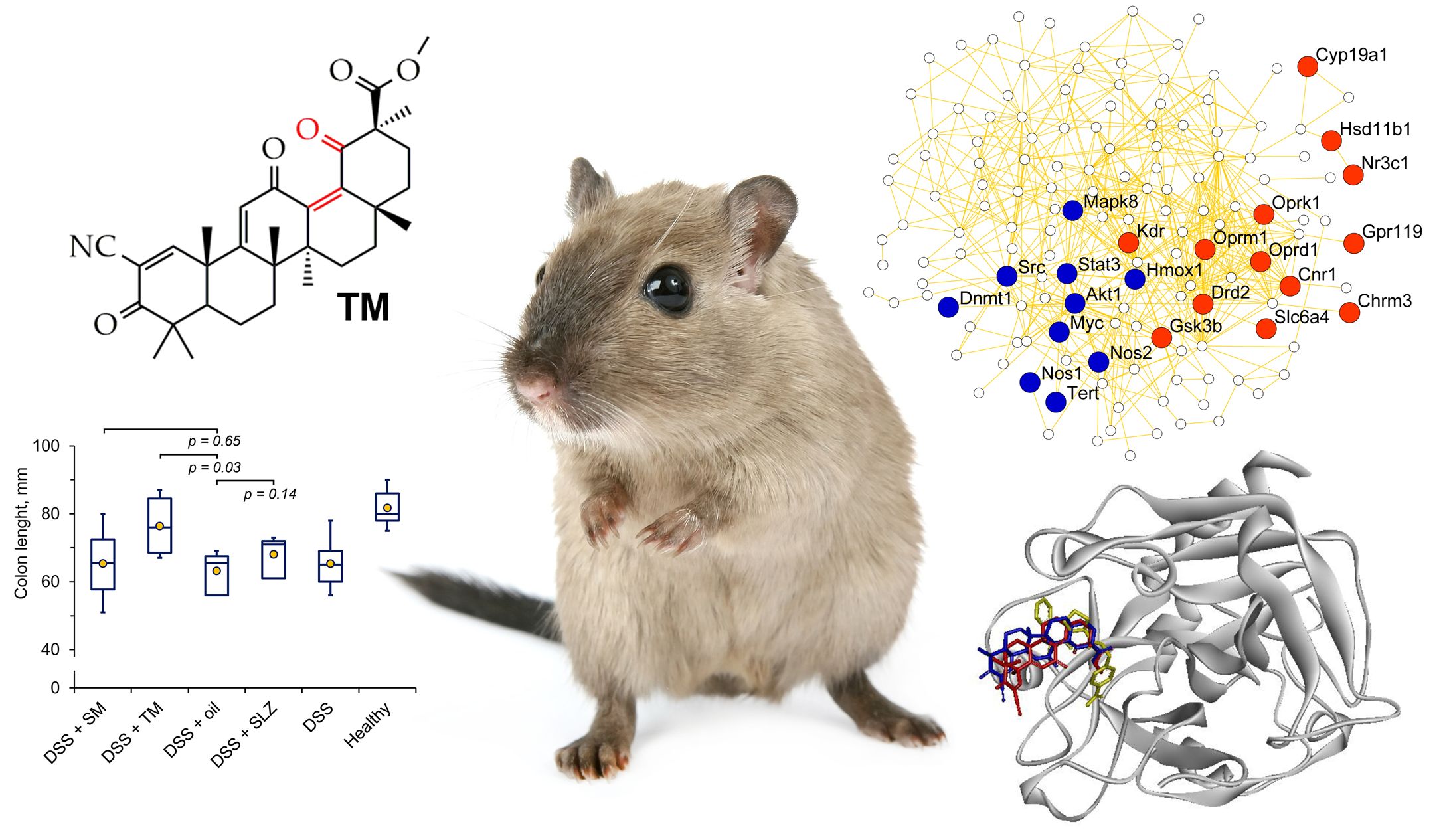
Слева сверху — структура триоксолон метила, слева снизу — график длины кишечника — чем он длиннее, тем лучше (при колите длина кишечника сокращается); справа сверху — генная ассоциативная сеть из потенциальных мишеней триоксолон метила (красные и синие круги) и генов, которые связаны с развитием колита (маленькие белые круги); справа снизу — одна из белковых мишеней триоксолон метила (видно, что и триоксолон метил (красная молекула), и солоксолон метил (синяя молекула) попадают при моделировании в сайт связывания известного ингибитора белка (желтая молекула). Рисунок предоставлен исследователями
«В результате наших исследований был не только разработан новый противовоспалительный препарат, но и показана тесная взаимосвязь между воспалением и злокачественной трансформацией тканей, — отмечает Андрей Марков. — Мы начали изучать активность триоксолон метила на колите в том числе и потому, что при длительном течении эта болезнь приводит к формированию аденом, а в дальнейшем — и к развитию колит-ассоциированного рака. Каким образом наш препарат воздействует на процессы онкотрансформации, мы будем смотреть в дальнейших исследованиях. Некоторые данные об этом уже есть, но эксперименты нужно повторить, чтобы убедиться в наличии активности».
Кроме того, с помощью биохимических и биофизических подходов необходимо доказать, что механизмы действия триоксолон метила, выявленные путем компьютерного моделирования, действительно реализуются в живых системах — на клетках и животных моделях.
Работа выполнена в рамках молодежного гранта РНФ Президентской программы «Проведение исследований научными группами под руководством молодых ученых». Недавно ученые получили продление этого гранта на следующие два года.
